

Año XXII. Edición 132. Diciembre Enero 2026
Intoxicación por tintura capilar. Manejo clínico del paciente felino. Reporte de Caso.
PALABRAS CLAVE: Felinos > intoxicación > tracto gastrointestinal > tintura capilar
María Fernanda Ávila Olivera¹
Diana Espinosa Flores²
-
Médico veterinario, Clínica Veterinaria del Bosque S.C.
-
pMVZ, Clínica Veterinaria del Bosque S.C.

Neumonía bacteriana
La mayoría de las intoxicaciones felinas son resultado de la ingestión y el contacto, dado que los gatos tienen un tamaño corporal más pequeño que los hace propensos a recibir dosis tóxicas más altas en función al peso y a que son deficientes de enzimas que permiten el metabolismo de tóxicos. En estos últimos años se ha observado un aumento de intoxicaciones felinas y aunque las causas más comunes se deben al consumo de rodenticidas, se han observado otros tipos de toxicosis tales como medicamentosas, inhalación de humos o químicas. Este artículo ofrece una perspectiva al manejo de intoxicación por tintura capilar y sus complicaciones en el paciente felino, las cuales representan un desafío de la vida clínica.

Resumen
De acuerdo con la Secretaría de Salud una intoxicación es la entrada de sustancias por exposición, ingesta, inyección o inhalación que pueden causar una lesión, enfermedad o muerte; si bien en la práctica veterinaria la incidencia de intoxicaciones es más alta en perros que en gatos, el manejo de intoxicaciones felinas es uno de los tantos retos que como médicos veterinarios tenemos diariamente debido a la complejidad y signos inespecíficos que los pacientes pueden desarrollar.
La especie felina, es deficiente de enzimas que permiten el metabolismo de tóxicos, tales como: UDP-glucuronosiltransferasa (UGT), deficiencia en la familia de las enzimas arilamina N-acetiltransferasa (NAT) citosólica, importantes para el metabolismo de aminas aromáticas y fármacos, baja actividad del aldehído oxidasa y de al menos dos enzimas clave del citocromo P450: CYP2B y CYP2C (Little, 2024). Por otro lado, de acuerdo con los Centros para el Control y Prevención de Enfermedades de Estados Unidos (CDC) y el Instituto Nacional del Cáncer (NCI), los tintes para cabello están compuestos de más de 5 mil sustancias químicas, algunas designadas como cancerígenas, entre estos compuestos se encuentran: naftilamina, compuestos amino-aromáticos, fenilendiaminas, diaminas de tolueno, arsénico, bismuto, alcohol desnaturalizado, acetato de plomo, mercurio amoniacal, pirogalol, plata y resorcinol, por nombrar algunos.
En estos últimos años se ha observado un aumento de intoxicaciones felinas y aunque las causas más comunes se debían al consumo de rodenticidas, se han observado otros tipos de toxicosis tales como medicamentosas, inhalación de humos o químicas (Markert et al., 2023) que ponen en riesgo la vida de nuestro paciente.
Presentación de caso clínico
Reseña y antecedentes
En estos últimos años se ha observado un aumento de intoxicaciones felinas y aunque las causas más comunes se debían al consumo de rodenticidas, se han observado otros tipos de toxicosis tales como medicamentosas, inhalación de humos o químicas (Markert et al., 2023) que ponen en riesgo la vida de nuestro paciente.
La paciente anteriormente había sido registrada en la base de datos del hospital debido al seguimiento y retiro de una neoplasia en el miembro pélvico izquierdo, misma que fue retirada el día 25 de octubre del 2024, para lo cual se evaluó previamente el día 12 de octubre del 2025 con pruebas de sangre (hemograma y química sanguínea) en donde los valores se encontraron sin alteraciones: RBC 10.63 M/μL, hematocrito 50.3%, hemoglobina 16.6 g/dL, reticulocitos 56.3 K/μL ; en cuanto a las células blancas se encontraron en rango (9.49 K/μL), neutrófilos (4.98 K/μL), linfocitos (3.87 K/μL), monocitos (0.22 K/μL), y plaquetas (272 K/μL).
Anamnesis
La propietaria refiere que el día 01 de noviembre por la noche empleo un tinte en aerosol de la marca Extasis® de color verde, se lo aplicó en el baño en donde en el piso quedaron residuos de este, sin darse cuenta, Morticia ingreso al baño en donde se quedó encerrada, posteriormente la tutora abrió el baño y encontró a la paciente adentro y notó que los residuos que habían quedado del tinte estaban desvanecidos. Durante la noche, Morticia se encontraba hecha “bolita”, triste y presentó alrededor de 10 vómitos.
1.Vómito
2.Letargo
3.Dolor abdominal
4.Fiebre
5.Deshidratación

Lista de problemas.
Durante la exploración la paciente se mostró alerta y responsiva, presentando fiebre (40°C), dolor a la palpación abdominal y deshidratación del 6%. El resto de las constantes fisiológicas se encontraron dentro de rangos clínicamente normales.
Exploración física.
Lista maestra.
I.Fiebre (2)
II.Vómito (2,3,5)
Diagnósticos diferenciales.
•Intoxicación por consumo de tintura capilar
•Enfermedad Infecciosa
•Enfermedad Metabólica
•Neoplasia / Metástasis
Diagnóstico presuntivo.
•Intoxicación por consumo de tintura capilar
Plan diagnóstico.
Se realizó hemograma y bioquímica sanguínea, en donde se reportó hiperglucemia (219 mg/dL), leucopenia (0.39 K/μL) debido a neutropenia (0.12 K/μL), linfopenia (0.15 K/μL), monocitopenia (0.02 K/μL), eosinopenia (0.06 K/μL) y trombocitopenia (129 K/μL). El RBC 9.45 M/μL, hematocrito 42.6%, hemoglobina 14.8 g/dL y reticulocitos 5.7 K/μL
En el ultrasonido abdominal se encotró engrosamiento de la pared gástrica e intestinal (Ver imagen 1 y 2)

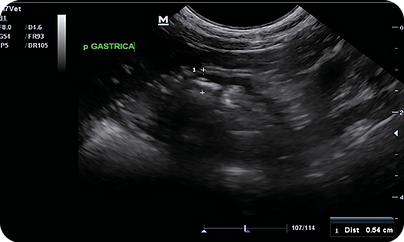
Imagen 1. Vista transversal, pared gástrica engrosada (1 cm), el grosor normal en gatos debe ser de 2-4mm.
Imagen 2. Vista transversal, pared intestinal engrosada (1 cm), los rangos normales varían desde 2.2 mm en duodeno y yeyuno, 2.8 mm en íleon y 1.5 mm en ciego y colón.
Plan terapéutico y evolución.
La paciente ingresó a hospitalización a las 14:00 hrs por intoxicación debido a la ingesta de tinte de cabello, el período que permaneció hospitalizada fue de 13 días.
Se implementó terapia de fluidos a un volumen constante de 17.5 ml/hr hasta nueva evaluación de deshidratación y se emplearon métodos físicos para disminuir la temperatura corporal (terapia de fluidos fría, ventiladores y compresas frías), así mismo se colocó una sonda de alimentación nasogástrica por la cual se administraba Recovery Liquid Dog & Feline de Royal Canin® 16 ml cada 2 hrs. Dentro del tratamiento inicial se incluyeron dexametasona (0.2 mg/kg) IV cada 24 hrs, buprenorfina (0.006 mg/kg) IV cada 8 hrs, citrato de maropitant (1mg/kg) IV cada 24 hrs, omeprazol (1 mg/kg) IV cada 24 hrs, sucralfato (0.5 g/paciente) PO cada 12 hrs, orniplural (1 mg/kg) IV cada 24 hrs, citicolina (50 mg/kg) IV cada 12 hrs.
Sin embargo, la paciente comenzó a presentar, dolor abdominal intenso, mucosas pálidas, hematemesis (imagen 3), hematoquecia (imagen 4) y fiebres intermitentes, entre el tercer y cuarto día de hospitalización. Es por esto por lo que al tratamiento se instauro:
Dipirona (15 mg/kg) IM cada 24 hrs, etamsilato (10 mg/kg) IV cada 8 hrs, hioscina (0.5 mg/kg) IV cada 8 hrs, ampicilina (25 mg/kg) IV cada 8 hrs y misoprostol (3 mcg/kg) PO cada 12 hrs. El misoprostol al ser comercializado en tabletas de 200 mcg se tuvo que redosificar con ayuda de un mortero y una micro balanza para dosificarlo en sobres de papel de 10.5 mcg.

Imagen 3.

Imagen 4.

Imagen 5. Trificación sanguinea de morticia

Imagen 6. Trificación sanguinea del donador.

Imagen 7. Morticia recibiendo transfusión sanguínea ( 70 ml )
Durante el control sanguíneo del día 08 de noviembre del 2024, el RBC se reportó en 2.40 M/μL hematocrito en 11.7%, hemoglobina en 3.7 g/dL y reticulocitos 13.7 K/μL, en la línea de células blancas se encontró leucocitosis (46.57 K/μL), asociado a linfocitosis (21.71 K/μL) y monocitosis (23.06 K/μL), neutropenia (1.44 K/μL) y trombocitopenia (29 K/μL). Motivo por el que se pidió autorización de la propietaria para realizar una transfusión sanguínea a la cual accedió. Se realizó tipificación sanguínea con una prueba RapidVet-H® Feline tanto para Morticia como para su donante. (Imagen 5, 6 y 7)
Al día siguiente de la transfusión la paciente comenzó a recibir alimento por si sola (lata ProPlan® Gastroenteric EN)
Para el día 10 de noviembre del 2024, se repitió un hemograma control en el que se reportó: RBC 2.66 M/μL, hematocrito 12.9%, hemoglobina 4.0 g/dL y reticulocitos 35.4 K/μL; en cuanto a las células blancas: leucocitosis (60.77 K/μL), asociado a linfocitosis (11.88 K/μL), monocitosis (3.01 K/μL) y neutrofilia (45.65 K/μL), eosinopenia (0.10 K/μL) y trombocitopenia (112 K/μL).
A pesar de que la paciente se encontraba recibiendo alimento y tanto el vómito como la diarrea habían parado, para el hemograma control que se realizó el 12 de noviembre del 2024, el RBC se encontraba en 2.23 M/μL, hematocrito 10.9% , hemoglobina 3.2 g/dL y reticulocitos 89 K/μL; células blancas: leucocitosis (33.90 K/μL), asociado a linfocitosis (7.40 K/μL), monocitosis (1.19 K/μL) y neutrofilia (25.02 K/μL), así como eosinopenia (0.11 K/μL).
Hacia el día 14 de noviembre del 2024, Morticia se reporta como un paciente estable, recibe agua y alimento por si sola y defeca sin presencia de sangre. Se corre un nuevo hemograma con los siguientes resultados: RBC 2.36 M/μL, hematocrito 11.5%, hemoglobina 3.3 g/dL, reticulocitos 101 K/μL; en cuanto a las células blancas: leucocitosis (33.73 K/μL), asociado a monocitosis (1.01 K/μL) y neutrofilia (27.54 K/μL), eosinopenia (0.13 K/μL).
Debido a la situación económica de la propietaria y que la paciente se encontraba clínicamente estable se decidió dar de alta voluntaria, con seguimiento ambulatorio y atención inmediata si presentaba alguna recaída.
En el hemograma control del día 16 de noviembre del 2024 se reportó: RBC 3.41 M/μL, hematocrito 17.2%, hemoglobina 4.9 g/dL y una reticulocitosis activa de 458.6 K/μL (13.5%), fecha en la que se consideró como una anemia regenerativa; en cuanto a las células blancas: leucocitosis (39.11 K/μL), asociado a neutrofilia (29.91 K/μL), linfocitosis (7.66 K/μL) y monocitosis (1.06 K/μL).
Para el 23 de noviembre del 2024 los resultados fueron los siguientes: RBC 6.78 M/μL, hematocrito 32.5%, hemoglobina 9.5 g/dL y reticulocitosis activa de 247.5 K/μL; en cuanto a las células blancas: leucocitosis (22.77 K/cL), asociado a neutrofilia (18.90 K/μL), monocitosis (1.14 K/μL) y trombocitosis (1290 K/μL).
La propietaria reportó evolución favorable de la paciente durante su estancia en casa, durante las revisiones subsecuentes los valores hematológicos de Morticia se encontraron estables y en proceso de regeneración, es así como el día 27 de enero del 2025 se realiza el último hemograma: RBC 11 M/μL, Hematocrito 43.6%, Hemoglobina 14.9 g/dL, reticulocitos 19.8 K/μL y leucocitos 9.32 K/μL sin alteración de ninguna línea celular blanca y Plaquetas 386 K/μL, por lo que se dio de alta médica a la paciente.
A continuación, se presentan los gráficos representativos al recuento celular de la línea roja y blanca reportada durante los hemogramas de control, previos a la hospitalización, durante y post hospitalario
En cuanto a la bioquímica sanguínea, se realizaron bioquímicas de control cada 4 días durante su estancia dentro del hospital:

Gráfico 1. Comportamiento del hematocrito de Morticia

Gráfico 2. Comportamiento de los reticulocitos en sangre, nótese que hubo un crecimiento exponencial para el día 16/11/2024, por lo que hasta ese momento se consideró como anemia regenerativa.
Discusión
Aunque el epitelio intestinal puede mantener la homeostasis normal en presencia de una exposición modesta o transitoria a estímulos nocivos, las interacciones de alto nivel o extensas con factores nocivos como la secreción excesiva de ácido gástrico e inflamación sustancial causada por enfermedades metabólicas o contenidos luminales tóxicos, pueden desestabilizar el equilibrio entre la lesión y la curación de la mucosa. Tras una lesión el tejido epitelial gastrointestinal (GI) es capaz de renovarse en cuestión de horas a meses, dependiendo del sitio, tamaño de la herida y el nivel epitelial al que se ha dañado el tejido, pues hay que considerar que la mucosa GI está protegida a tres niveles: defensas pre epiteliales, epiteliales y subepiteliales. (Oncel, 2022).
06/11/2024. Hiperglucemia 202 mg/dL, creatinina 0.5 mg/dL, hipoalbuminemia 1.9 g/dL, ALP <10 U/L, hiperbilirrubinemia 1.2 mg/dL
08/11/2024. Hiperglucemia 316 mg/dL, creatinina 0.6 mg/dL, hipocalcemia 7.5 mg/dL, hipoproteinemia 4.3 g/dL causada por hipoalbuminemia 1.6 g/dL y globulina 2.7 g/dL, ALP <10 U/L, GGT 11 U/L, hiperbilirrubinemia 1.6 mg/dL
12/11/2024. Hiperglucemia 217 mg/dL, creatinina 0.5 mg/dL, BUN 15 mg/dL, hipoproteinemia 4.8 g/dL causada por hipoalbuminemia 1.7 g/dL, ALP <10 U/L
23/11/2024. Creatinina 0.7 mg/dL, hiperamilasemia 1,715 U/L

Gráfico 3. Comportamiento plaquetario en sangre.

Gráfico 4. Comportamiento de la línea celular blanca
Como anteriormente se mencionó, el tinte capilar que la paciente ingirió tiene como principal ingrediente etanol o alcohol etílico, el cual es uno de los alcoholes que con mayor frecuencia causan intoxicaciones a los animales de compañía y por sí solo es capaz de contribuir a la ulceración de la mucosa gastrointestinal al atraer citocinas inflamatorias que a su vez facilitan la generación de especies reactivas de oxígeno (ROS), produciendo estrés oxidativo y agravando el daño tisular gástrico (Ahmed, 2024). De igual manera se ha demostrado que este compuesto tiene efectos adversos sobre el sistema inmune, asociados principalmente a actividades proinflamatorias, sin embargo se ha planteado que la deficiencia de la enzima ALDH y sus isoformas (ALDH2, ALDH1A1 y ALDH3A1), así como una sobreexposición al metabolito del etanol: acetaldehído, causa un mayor riesgo de hematopoyesis alterada asociada a la formación de aductos de ADN y la inhibición de la reparación del ADN por déficit del gen Fancd2 (Brooks & Zachari, 2013; Smith et al., 2015).
Otros ingredientes como el propano butano, al consumirse son rápidamente absorbidos por tejidos con alta concentración de lípidos como cerebro, bazo, hígado y riñón (Rossi et al., 2012; Sironi et al., 2016; Vahabzadeh & Mégarbane, 2022). Esta inhalación o consumo del tóxico conduce a una liberación masiva de catecolaminas (noradrenalina, epinefrina y dopamina) (Sironi et al., 2016; Vahabzadeh & Mégarbane, 2022), las cuales causan efectos adversos sobre diferentes órganos y vías de metabolismo, en especial sobre el de la glucosa, en la que la epinefrina promueve la glucogenólisis en el hígado y músculo esquelético, inhibe la secreción de insulina de las células β del páncreas y estimula la secreción de glucagón de parte del páncreas aumentando la concentración de glucosa en sangre (Klein, 2020).
Ingredientes como el dióxido de titanio (TiO2) y la tartrazina, son catalogados como cancerígenos y mutagénicos al consumirse de manera masiva (Khan et al., 2024 y Barciela et al., 2023; Pay et al., 2023). Ambos compuestos causan daño directo al epitelio gastrointestinal al ser ingeridos, ya que promueven la generación de ROS y disminución de la expresión de moléculas antioxidantes: superóxido dismutasa (SOD), catalasa (CAT) y glutatión reducido (GSH), eventos que desencadenan en estrés oxidativo e inflamación que en última instancia conducirán a daño en el ADN, aumentando la expresión de genes proapoptóticos como p53, Bax, Factor de Necrosis Tumoral alfa (TNF-α), caspasas-8,9 y 3, en el caso de TiO2 y provocando sobreexpresión de las citocinas proinflamatorias (IL 1 y 6 ), lisozimas de tipo c (CLYZ), el componente 3 del complemento (C3) y la β-defensina 3 como efecto de la tartrazina (Khan et al., 2024; Ma et al., 2023; Zhang et al., 2023 y Amchova et al., 2024; Khayyat et al., 2017; Wu et al., 2021).
Este consumo masivo de ingredientes altamente tóxicos causó una reacción inflamatoria generalizada del tracto gastrointestinal que evolucionó hasta convertirse en gastroenteritis ulcerativa, provocando hematemesis y hematoquecia, por lo que el tratamiento para estos eventos se centran en la regeneración del epitelio GI, con la administración de fármacos que promuevan además la generación de enzimas antioxidantes; es así como el uso de sucralfato y misoprostol entran con un papel clave para la resolución de este caso. Ya que el sucralfato actúa formando complejos estables con proteínas en la mucosa dañada, también interfiere con la acción de la pepsina ya sea uniéndose a ella o proporcionando una barrera que impide su difusión (Bhatia & Lodha, 2010; Hershcovici & Fass, 2011). Además, se ha postulado que el sucralfato estimula la producción de prostaglandinas E2 e I2 (prostaciclina), junto con la secreción de moco y bicarbonato, lo que ofrece efectos citoprotectores adicionales (Bazelle et al., 2018). Esta prostaglandina I2 (PGI2) o prostaciclina interviene en la reparación de la mucosa gastrointestinal, al ser la prostaglandina más abundante en la mucosa gástrica, se ha sugerido que una de las acciones citoprotectoras la da al inhibir la activación leucocitaria aumentando los niveles intracelulares de Adenosín Monofosfato cíclico (AMPc) (Harada et al., 1999) y aumentando el flujo sanguíneo de la mucosa (Chu et al., 2015), se ha observado que de forma in vitro los análogos de PGI2 aumentan la producción de IL-10 antiinflamatoria y disminuyen la producción de TNF-α, IL-1α , IL-6 e IL-12 (Dorris & Peebles, 2012).
Sumado a este efecto del sucralfato, el misoprostol es un fármaco análogo sintético de la prostaglandina E1 (PGE1), desarrollado para la prevención y tratamiento de las úlceras pépticas debido a sus propiedades antisecretoras del ácido gástrico (Tang et al., 2007). PGE1 posee actividades inmuno inhibitorias, incluida la regulación negativa de la producción de ROS, supresión de la producción de citocinas proinflamatorias, la inhibición de leucocitos y la migración endotelial (Yang, 2002), así mismo se ha reportado que es capaz de disminuir las concentraciones de Malondialdehído (MDA), aumentar los niveles de GSH y la actividad de CAT y SOD e interviene en la prevención del aumento de los niveles tisulares de la caspasa 3 (CASP-3) (Aktas & Yahyazadeh, 2022; Bilgic & Armagan, 2019). Logra su efecto aumentando los factores esenciales para la integridad de la mucosa gastroduodenal, uniéndose a las células parietales en el estómago, reduciendo el volumen, la concentración y la secreción de ácido; ya que es análogo de PGE1 también tiene una potente propiedad vasodilatadora a altas concentraciones (Aktas & Yahyazadeh, 2022; Bazelle et al., 2018) disminuye la histamina, pentagastrina y la secreción ácida gástrica estimulada por el consumo de alimento; al unirse a los receptores de prostaglandinas además inhibe la formación de Adenosín Monofosfato cíclico (AMPc) estimulado por la histamina que en consecuencia contribuye a la reducción de la proliferación y producción de citocinas proinflamatorias (Marks et al., 2018). Adicionalmente, los efectos citoprotectores del misoprostol se deben al aumento de la secreción del bicarbonato, disminución del contenido de pepsina en la secreción gástrica, la preservación de las uniones estrechas entre las células epiteliales, el aumento de la secreción mucosa, aumento del flujo sanguíneo mucoso y la mejora de la capacidad regenerativa de la mucosa (Marks et al., 2018; Oncel, 2022; Ozer et al., 2011).
Aunque inicialmente el tratamiento incluía omeprazol, este se retiró debido a que, aunque se encuentre indicado para el tratamiento de úlceras sangrantes, al ser un inhibidor de la bomba de protones (IBP) actúa manteniendo el pH estomacal por encima de 4.0 durante más de 10 hrs en promedio y este aumento de pH puede modificar la absorción y biodisponibilidad de otros fármacos dependientes de pH (Ghezala et al., 2022; Miner et al., 2003) tales como el sucralfato; además parece que la inhibición ácida por IBP es insuficiente para una cicatrización exitosa de alta calidad de la úlcera gastroduodenal debido a los niveles bajos de prostaglandinas y los niveles altos de radicales libres de oxígeno implican una mala calidad de la curación de la úlcera (Oncel, 2022)
Y aunque la recuperación de la paciente fue exitosa, no se debe descartar la posibilidad de mielosupresión causada por el consumo del etanol, ya que como se mencionó anteriormente, existe evidencia de que la sobreexposición al acetaldehído puede general hematopoyesis alterada, esta idea es meramente una hipótesis basada en la investigación y evidencia laboratorial, tales como linfopenia súbita y anemia normocítica normocrómica no regenerativa durante la enfermedad que pudieron alterar la recuperación de la paciente, sin embargo se necesitan más estudios y pruebas de laboratorio para corroborarlo.
Conclusión
El correcto uso de protectores de la mucosa, IBP y fármacos como el misoprostol son la clave para lograr la restauración del epitelio GI, tomando en cuenta los factores que causaron la patología que el paciente curse. Por otro lado, con la evidencia recabada, no se debe tomar a la ligera la exposición a ciertos tóxicos de uso cotidiano a los felinos, ya que incluso la ingesta mínima puede desencadenar una serie de eventos fatídicos que pueden causar la muerte del individuo, por lo que la terapia de soporte y la tolerancia de la paciente fueron claves para su supervivencia. Por último, no se debe descartar las posibles implicaciones negativas de los ingredientes tóxicos a la médula ósea que pudieron interferir en la condición de Morticia al retrasar su respuesta inmunitaria, por lo que en casos similares la evaluación de esta podría ser la clave para la supervivencia del paciente.
Bibliografía
-
Ahmed, Z. A. (2024, Noviembre). Gastroprotective Effect of Quercetin and Misoprostol in Ethanol-Induced Gastric Ulcer in Rats. Turkish Journal of Gastroenterology, 35(11), 822-830. PubMed. 10.5152/tjg.2024.24209
-
Aktas, I., & Yahyazadeh, A. (2022, Diciembre). Protective potential of misoprostol against kidney alteration via alleviating oxidative stress in rat following exposure to paclitaxel. Tissue and Cell, 79, 101966. ScienceDirect. https://doi.org/10.1016/j.tice.2022.101966
-
Amchova, P., Siska, F., & Ruda-Kucerova, J. (2024, Septiembre 19). Safety of tartrazine in the food industry and potential protective factors. Heliyon, 10(18), e38111. PubMed. https://doi.org/10.1016/j.heliyon.2024.e38111
-
Barciela, P., Pérez-Vázquez, A., & Prieto, M.A. (2023, Agosto). Azo dyes in the food industry: Features, classification, toxicity, alternatives, and regulation. Food and Chemical Toxicology, 178, 113935. PubMed. https://doi.org/10.1016/j.fct.2023.113935
-
Bazelle, J., Threlfall, A., & Whitley, N. (2018, Octubre). Gastroprotectants in small animal veterinary practice – a review of the evidence. Part 1: cyto-protective drugs. Journal Of Small Animal Practice, 59(10), 587 - 602. PubMed. https://doi.org/10.1111/jsap.12867
-
Bhatia, V., & Lodha, R. (2010, Diciembre 11). Upper -Gastrointestinal Bleeding. The Indian Journal of Pediatrics, 78, 227 - 233. PubMed. 10.1007/s12098-010-0296-6
-
Bilgic, S., & Armagan, I. (2019, Agosto 20). Effects of misoprostol treatment on doxorubicin induced renal injury in rats. Biotechnic & Histochemistry, 95(2), 113-120. PubMed. https://doi-org.pbidi.unam.mx:2443/10.1080/10520295.2019.1645356
-
Brooks, P.J., & Zachari, S. (2013). Acetaldehyde and the -genome: Beyond nuclear DNA adducts and carcinogenesis. Environmental And Molecular Mutagenesis,, 55(2), 77 - 91. PubMed. https://doi.org/10.1002/em.21824
-
Chu, L., Liou, J.-Y., & Wu, K. K. (2015, Abril - Junio). Prostacyclin protects vascular integrity via PPAR/14-3-3 pathway. Prostaglandins & Other Lipid Mediators, 118 -119, 19 - 27. ScienceDirect. https://doi.org/10.1016/j.prostaglandins.2015.04.006
-
Dorris, S. L., & Peebles, R. S. (2012). PGI 2 as a Regulator of Inflammatory Diseases. Mediators of Inflammation, 926968. PubMed. https://doi-org.pbidi.unam.mx:2443/10.1155/2012/926968
-
Ghezala, I. B., Luu, M., & Bardou, M. (2022, Julio 11). An update on drug–drug interactions associated with proton pump inhibitors. Expert Opinion on Drug Metabolism & Toxicology, 18(5), 337 - 346. PubMed. https://doi-org.pbidi.unam.mx:2443/10.1080/17425255.2022.2098107
-
Harada, N., Okajima, K., Murakami, K., Isobe, H., & Liu, W. (1999, Julio). Gastric prostacyclin (PGI2) prevents stress-induced gastric mucosal injury in rats primarily by inhibiting leukocyte activation. Prostaglandins & Other Lipid Mediators, 57(5 - 6), 291 - 303. ScienceDirect. https://doi.org/10.1016/S0090-6980(98)00077-X
-
Hershcovici, T., & Fass, R. (2011, Abril). Pharmacological management of GERD: where does it stand now? Trends in Pharmacological Sciences, 32(4), 258 - 264. Science Direct. https://doi.org/10.1016/j.tips.2011.02.007
-
Khan, J., Kim, N. D., Bromhead, C., Truman, P., Kruger, M. C., & Mallard, B. L. (2024, Mayo 13). Hepatotoxicity of titanium dioxide nanoparticles. Journal Of Applied Toxicology., 45(1), 23-46. Wiley Analytical Science. https://doi.org/10.1002/jat.4626
-
Khayyat, L., Essawy, A., Sorour, J., & Soffar, A. (2017, Febrero 23). Tartrazine induces structural and functional aberrations and genotoxic effects in vivo. PeerJ, 5, e3041. PubMed. https://doi.org/10.7717/peerj.3041
-
Klein, T.B.G. (2020). Cunningham. Fisiología veterinaria. (6th ed., Vol. 6). Elsevier Health Sciences.
-
Little, S. (2024). The Cat (2nd ed.). Elsevier Health Sciences.
-
Ma, Y., Yu, N., Lu, H., Shi, J., Zhang, Y., Chen, Z., & Jia, G. (2023, Junio 22). Titanium dioxide nanoparticles: revealing the mechanisms underlying hepatotoxicity and effects in the gut microbiota. Archives Of Toxicology, 97, 2051-2067. PubMed. https://doi.org/10.1007/s00204-023-03536-x
-
Markert, C., Heilmann, R. M., Kiwitz, D., & Dörfelt, R. (2023). A retrospective evaluation of confirmed and suspected poisonings in 166 cats between 2016 and 2020. Veterinary world, 16(9), 1940–1951. https://doi.org/10.14202/vetworld.2023.1940-1951
-
Marks, S. L., Kook, P. H., Papich, M. G., Tolbert, M., & Willard, M. D. (2018, Noviembre / Diciembre). ACVIM consensus statement: Support for rational administration of gastrointestinal protectants to dogs and cats. Journal Of Veterinary Internal Medicine, 32(6), 1823 - 1840. PubMed. https://doi.org/10.1111/jvim.15337
-
Miner, P. J., Katz, P. O., Chen, Y., & Sostek, M. (2003, Diciembre). Gastric Acid Control With Esomeprazole, Lansoprazole, Omeprazole, Pantoprazole, and Rabeprazole: A Five-Way Crossover Study. American Journal of Gastroenterology, 98(12), 2616 - 2620. PubMed. https://doi-org.pbidi.unam.mx:2443/10.1111/j.1572-0241.2003.08783.x
-
Oncel, S. (2022, Mayo 7). Gut homeostasis, injury, and healing: New therapeutic targets. World Journal of Gastroenterology, 28(17), 1725 - 1750. PubMed. https://doi.org/10.3748/wjg.v28.i17.1725
-
Ozer, M. K., Asci, H., Oncu, M., Calapoglu, M., Savran, M., Yesilot, S., Candan, I. A., & Cicek, E. (2011, Julio). Effects of misoprostol on cisplatin-induced renal damage in rats. Food and Chemical Toxicology, 49(7), 1556 - 1559. ScienceDirect. https://doi.org/10.1016/j.fct.2011.03.051
-
Pay, R., Sharrock, A. V., Elder, R., Maré, A., Bracegirdle, J., Torres, D., Malone, N., Vorster, J., Kelly, L., Ryan, A., Josephy, P. D., Allen-Vercoe, E., Ackerley, D. F., Keyzers, R. A., & Harvey, J. E. (2023, Diciembre). Preparation, analysis and toxicity characterisation of the redox metabolites of the azo food dye tartrazine. Food and Chemical Toxicology, 182, 114193. PubMed. https://doi.org/10.1016/j.fct.2023.114193
-
Rossi, R., Suadoni, F., Pieroni, L., De-Giorgio, F., & Lancia, M. (2012, Mayo). Two Cases of Acute Propane/Butane Poisoning in Prison. Journal Of Forensic Sciences, 57(3), 832 - 834. Wiley Online Library.
-
Sironi, L., Amadasi, A., & Zoja, R. (2016, Septiembre). Recreational inhalation of butane and propane in adolescents: Two forensic cases of accidental death. Forensic Science International, 266, e52 - e58. ScienceDirect. https://doi.org/10.1016/j.forsciint.2016.05.028
-
Smith, C., Gasparetto, M., Jordan, C., Pollyea, D. A., & Vasiliou, V. (2015). Biological Basis of Alcohol-Induced Cancer (349 - 359 ed.). Springer. https://doi.org/10.1007/978-3-319-09614-8_20
-
Tang, S. O., Gemzell-Danielsson, K., & Ho, P. (2007, Diciembre). Misoprostol: Pharmacokinetic profiles, effects on the uterus and side-effects. International Journal of Gynecology & Obstetrics, 99(S2), S160-S167. PubMed. https://doi-org.pbidi.unam.mx:2443/10.1016/j.ijgo.2007.09.004
-
Vahabzadeh, M., & Mégarbane, B. (2022, Septiembre). A two-decade review of butane toxicity as a substance of abuse. Basic & Clinical Pharmacology & Toxicology, 131(3), 155 - 164. Wiley Online Library. https://doi.org/10.1111/bcpt.13760
-
Wu, L., Nivel, X., Zhang, Y., Xin, Q., Zou, Y., & Li, X. (2021, Diciembre). Tartrazine exposure results in histological damage, oxidative stress, immune disorders and gut microbiota dysbiosis in juvenile crucian carp (Carassius carassius). Aquatic Toxicology, 241, 105998. PubMed. https://doi.org/10.1016/j.aquatox.2021.105998
-
Yang, H. (2002, Julio). Prostaglandin E1 Protects Human Liver Sinusoidal Endothelial Cell from Apoptosis Induced by Hypoxia Reoxygenation. Microvascular Research, 64(1), 94-103. ScienceDirect. https://doi.org/10.1006/mvre.2002.2404
-
Zhang, X., Song, Y., Gong, H., Wu, C., Wang, B., Chen, W., Hu, J., Xiang, H., Zhang, K., & Sun, M. (2023, Diciembre 5). Neurotoxicity of Titanium Dioxide Nanoparticles: A Comprehensive Review. International Journal Of Nanomedicine, 18, 7183-7204. PubMed. https://doi.org/10.2147/ijn.s442801
